Kimyasal reaksiyonların hızını etkileyen birkaç faktör olduğunu hepimiz biliyoruz. Bunları kısaca bir hatırlamak gerekirse başlıklar şu şekilde olacaktır:
- Konsantrasyon
- Basınç
- Parçacık Boyutu
- Sıcaklık
- Katalizörün varlığı
Konsantrasyonun Kimyasal Reaksiyon Oranına Etkisi
Bir veya daha fazla reaktantın (tepkimeye giren ürünler) konsantrasyonundaki bir artış reaksiyon hızını arttıracaktır. Neden mi?
Bir veya daha fazla reaktantın konsantrasyonu arttığında aşağıdaki olaylar dizisi meydana gelir:
- Belirli bir hacimde daha fazla reaktant partikülü olacaktır. (Yani birim hacim başına çok daha fazla sayıda reaktant partikülü)
- Reaktant molekülleri daha sık çarpışacaktır.
- Birim hacim başına çarpışma sayısı artacaktır.
- Etkili çarpışma sayısı artacaktır.
- Reaksiyon hızı artacaktır.
Ufak bir örnek ile bu durumu açıklamak gerekirse; bir basketbol maçının 5’er kişiden oluşan takımlardan değilde 10’ar kişiden oluşan takımlardan oynandığını düşünün. Sahanın içerisinde çok daha fazla birbiri ile çarpışacak insan olacaktır (reaktantlar). Dolayısı ile çarpışma sıklıkları artacaktır. Daha çok insan çarpıştığı için daha çok düşmeler, yaralanmalar olacaktır (reaktantlar arasında gerçekleşen tepkime artacaktır).
Basıncın Kimyasal Reaksiyon Oranına Etkisi
Basınçtaki bir değişiklik sadece gaz halindeki reaktantları içeren kimyasal reaksiyonlar için reaksiyon hızını etkiler. Basınçtaki bir artış, reaksiyon hızında bir artışa yol açacaktır. Neden?
Basınç arttığında aşağıdaki olaylar dizileri ortaya çıkar:
- Basınçtaki artış, gaz halindeki reaktant partiküllerini birbirine yaklaştırır.
- Birim hacim başına reaktif parçacık sayısı artar.
- Birim hacim başına çarpışma sayısı artacaktır.
- Etkili çarpışma sayısı artar.
- Reaksiyon hızı artar.
Kimyasal reaksiyonların hızını arttırmak için endüstriyel işlemlerde yüksek basınç sıklıkla kullanılır. Bunun nedeni, daha yüksek bir reaksiyon oranının birim zaman başına daha fazla ürünün yapıldığı (yani şirketler için daha fazla kar) anlamına gelmesidir. Böyle bir endüstriyel işlemin yaygın bir örneği Haber-Bosch prosesi ile amonyak üretim sürecidir. Burada işlemi hızlandırmak ve verimi arttırmak için 200 atm’lik bir basınç kullanılır.
Basınç biraz can sıkıntısı gibi değil mi sizce de ? Hani canınız sıkılır da yerinizde duramazsınız bir türlü. Bir sağa, bir sola gidersiniz sürekli.. Stres gibi.. Ama işin sonunda daha çok hareket varsa, daha çok reaksiyon var.
Parçacık Boyutunun Kimyasal Reaksiyon Oranına Etkisi
Katı bir reaktantın partikül boyutunda bir azalma reaksiyon hızını arttıracaktır. Neden ?
Katı bir reaktantın parçacık boyutu azaldığında,aşağıdaki olaylar dizisi meydana gelebilir:
- Katı bir reaktantın parçacık boyutu, katı reaktantın daha küçük parçalara parçalanması ile azalır.
- Bu işlem sonunda toplam yüzey alanını artar.
- Reaktant parçacıkları arasındaki temas alanı artar.
- Birim zamanda çarpışma sayısı artar.
- Birim zamandaki etkin çarpışma sayısı artar.
- Reaksiyon hızı artar.
Sanırım bu konu biraz şunun gibi. 5 uzun boylu basketbolcunun oyundan çıkıp yerine 10 kısa boylu basketbolcu girmesi gibi.. Aynı ortamda daha fazla oyuncu olacağı için çarpışma sayısı ve dolayısı ile reaksiyon hızı ister istemez artacaktır.
Sıcaklığın Kimyasal Reaksiyon Oranına Etkisi
Sıcaklıktaki bir artış, çoğu kimyasal reaksiyonun reaksiyon hızını arttıracaktır. Neden ?
Sıcaklık arttırıldığında,aşağıdaki olaylar dizisi meydana gelebilir:
- Reaktant partikülleri daha fazla kinetik enerjiye sahip olurlar. Yani daha hızlı hareket ederler.
- Reaktant partikülleri arasındaki çarpışma sıklığı artar ve daha fazla sayıda reaktant partikülü aktivasyon enerjisine eşit veya daha fazla enerjiye sahip olur.
- Birim zamanda çarpışma sayısı artar.
- Birim zamandaki etkin çarpışma sayısı artar.
- Reaksiyon hızı artar.
Kaynayan suyu izlediniz mi hiç ? Su molekülleri yerinde duramaz, çıldırmış gibi hareket ederler.. Hiç normal anlarında durdukları gibi sakince durmazlar..
Katalizörün Kimyasal Reaksiyon Oranına Etkisi
Katalizör, reaksiyonun sonunda herhangi bir kalıcı kimyasal değişikliğe uğramadan reaksiyon hızını değiştiren maddelere denir.
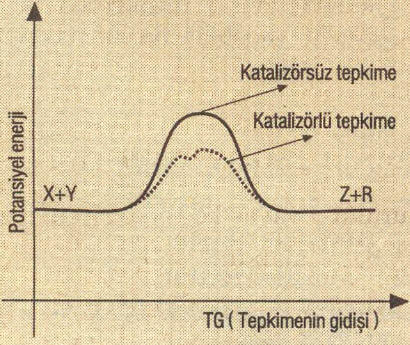
Bir katalizör, reaksiyon için alternatif bir reaksiyon yolu, yani çok daha düşük bir aktivasyon enerjisine sahip bir yol sağlayarak çalışır. (Yukarıdaki şekilde gösterildiği gibi).
Bu şu anlama gelir: Ortamda bir katalizörün varlığı reaksiyon hızını arttıracaktır. Neden?
Bir katalizör ile aşağıdaki olaylar dizisi meydana gelebilir:
- Daha düşük bir aktivasyon enerjisine sahip alternatif reaksiyon yolu şimdi uygundur.
- Daha reaktif parçacıklar,enerji bariyerinin üstesinden gelmek için yeterli enerjiye sahip olacaktır.
- Birim zamandaki etkin çarpışma sayısı artar.
- Reaksiyon hızı artar.
Katalizörü üşengeç bir arkadaş gibi düşünebilirsiniz. Ona yapması için bir iş verin ve işin daha kolay bir yoldan nasıl yapılacağını bulsun ve size söylesin..
Katalizörler hakkındaki notlar;
- Bir katalizör reaksiyon sonunda kimyasal olarak değişmeden kalsa da, renk ve doku gibi fiziksel özellikleri değiştirilebilir. (Örneğin siyah katı bir madde reaksiyon sonunda toz haline getirilebilir.)
- Bir katalizör genellikle eylemde spesifiktir. Yani sadece bir tip reaksiyonu katalizleyebilir. Farklı reaksiyonlar farklı türde katalizörlere ihtiyaç duyacaktır.
- Bir katalizör, kimyasal reaksiyonda oluşan ürün tiplerini veya miktarını etkilemez. Sadece ürünlerin daha kısa sürede elde edilmesini sağlar.
- Geçiş metalleri ve onların bileşikleri iyi katalizörler oluştururlar.
- Enzimler biyolojik katalizörlerdir.


